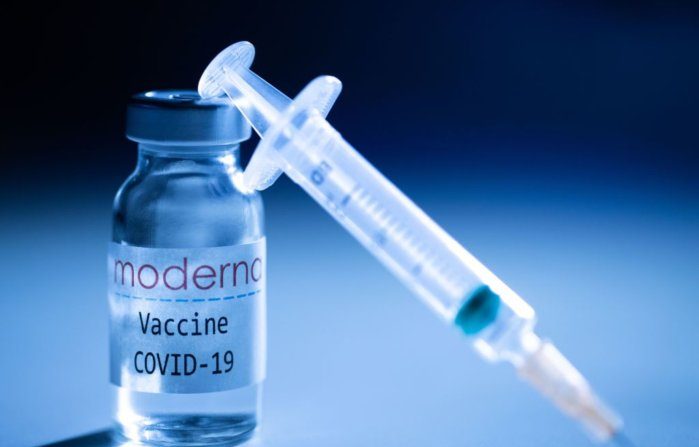
Un vaccino sviluppato congiuntamente da Moderna e dall’Istituto Nazionale di Sanità statunitense (Nih) avrebbe mostrato un’efficacia pari al 94,5 percento.
L’azienda di biotecnologia Moderna ha dichiarato in un comunicato stampa di lunedì che un’analisi clinica della sua sperimentazione, effettuata da un comitato indipendente di monitoraggio dei dati, dimostra che il suo vaccino sperimentale è altamente efficace nel prevenire l’infezione da parte del nuovo coronavirus, anche noto come virus del Pcc (Partito Comunista Cinese).
La Nih ha dichiarato in un comunicato separato che «i risultati sono statisticamente significativi, il che significa che probabilmente non sono dovuti al caso. Questa analisi intermedia dei dati suggerisce che il vaccino è sicuro ed efficace nel prevenire i sintomi del Covid-19 negli adulti».
La sperimentazione del vaccino ha coinvolto più di 30 mila partecipanti negli Stati Uniti, con metà delle persone che hanno ricevuto due dosi di vaccino a 28 giorni di distanza l’una dall’altra, mentre l’altra metà ha ricevuto due dosi di placebo.
Il vaccino combina la biotecnologia basata sull’Rna messaggero di Moderna con la proteina spike immunogena del Sars-Cov-2 sviluppata dagli scienziati dell’Istituto nazionale per le allergie e le malattie infettive (Niaid), che fa parte del Nih.
Stéphane Bancel, amministratore delegato di Moderna, ha dichiarato in un comunicato: «Questo è un momento cruciale per lo sviluppo del nostro candidato al vaccino Covid-19. Questa positiva analisi intermedia della Fase 3 del nostro studio ci ha dato la prima conferma clinica che il nostro vaccino può prevenire la malattia del Covid-19, inclusa la forma grave. […] Questa traguardo è stato possibile solo grazie al duro lavoro e ai sacrifici di tanti».
Di fatto, lo studio per il vaccino è realizzato in collaborazione con l’Nih, il Niaid e la Biomedical Advanced Research and Development Authority (Barda), che fa parte del Dipartimento della Salute e dei Servizi Umani statunitense.
«Voglio ringraziare i nostri partner della Barda e dell’Operazione Warp Speed che sono stati fondamentali per accelerare i nostri progressi fino a questo punto», ha aggiunto Bancel, riferendosi agli sforzi del governo Trump per accelerare lo sviluppo, la produzione e la distribuzione di un vaccino effiace contro il Covid-19.
Moderna ha anche dichiarato che ha intenzione di presentare una richiesta d’emergenza per l’autorizzazione del suo vaccino alla Food and Drug Administration nelle prossimi settimane.
«Non vediamo l’ora di completare i prossimi passi per la presentazione di una Eua [Emergency Use Authorization, ndt] negli Stati Uniti, e per la presentazione delle domande di autorizzazione nei Paesi di tutto il mondo, mentre continuiamo a raccogliere dati sulla sicurezza e l’efficacia del vaccino nello studio [denominato, ndt] Cove – ha dichiarato Bancel – Rimaniamo impegnati e concentrati nel fare la nostra parte per contribuire a porre fine alla pandemia di Covid-19».
L’azienda ha detto che si aspetta di poter consegnare circa 20 milioni di dosi del suo vaccino negli Stati Uniti entro la fine del 2020 e che l’anno prossimo, si aspetta di poter rendere disponibili tra i 500 milioni e il miliardo di dosi in tutto il mondo.
Contando il vaccino di Pfizer, che sembra avere un’efficacia superiore al 90 percento, gli Stati Uniti potrebbero avere due vaccini autorizzati per l’uso d’emergenza già a dicembre, con addirittura 60 milioni di dosi di vaccino disponibili quest’anno.
Un vantaggio fondamentale del vaccino di Moderna è che, a differenza di quello di Pfizer, non ha bisogno di essere conservato a temperature molto basse, rendendone più facile la distribuzione.
Al 16 novembre, i casi di contagio hanno superato gli 11 milioni negli Stati Uniti, di cui un milione registrati solo nell’ultima settimana.
Articolo in inglese: Moderna CCP Virus Vaccine Nearly 95 Percent Effective